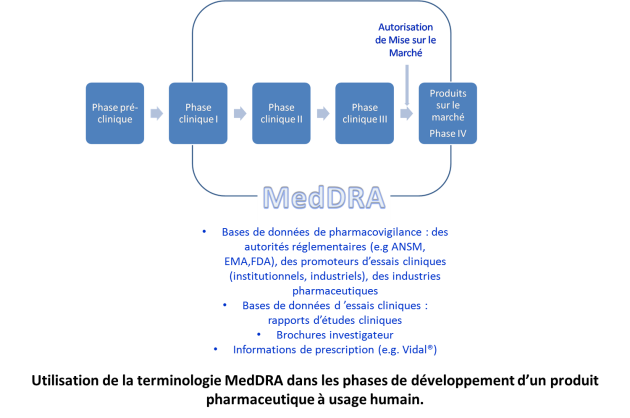
Utilisation
Il est utilisé pour l'ensemble des aspects réglementaires qui concerne les produits pharmaceutiques à usage humain, avant et après leur commercialisation, de la saisie des données (codage), en passant par leur évaluation, leur présentation, la transmission et la déclaration des effets/évènements indésirables